カスタムスペクトルライブラリを検索対象とした抗酸菌群(Mycobacteria)の同定
質量分析法により、培養が困難な細菌や増殖速度の遅い細菌を迅速に同定する事ができます。迅速な同定は患者に速やかな治療の提供を可能とします。その中でも最も迅速な同定法は、種に特異的なペプチド配列を集めたスペクトルライブラリ(SL)に対して測定したMS/MSスペクトルデータを検索する方法でしょう。この記事では、独自に作成した抗酸菌(Mycobacteria)スペクトルライブラリの構築手順と、Mascot Serverでの使用方法について詳しく説明します。
抗酸菌群[マイコバクテリア]の同定
同定が困難な細菌群の一つとしてMycobacteria 属が挙げられます。約195種の桿状グラム陽性細菌からなり、ペプチドグリカンとアラビノガラクタンからなる厚く疎水性でミコール酸を豊富に含む細胞壁を有しています。これらが病原体となるヒトの病気として、結核(M. tuberculosis)およびハンセン病(M. leprae)があります。こういった病気を引き起こさないその他のマイコバクテリウムは、「非結核性マイコバクテリウム(NTM, NonTuberculous Mycobacteria)」として知られています。
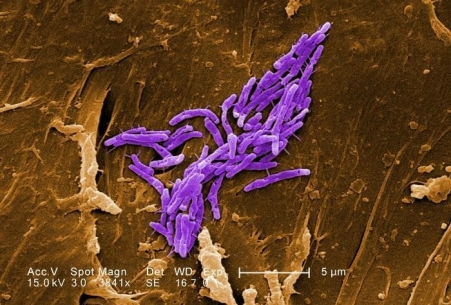
走査型電子顕微鏡(SEM)による3841倍拡大のMycobacterium fortuitum(デジタル着色)。
抗酸菌群[マイコバクテリア]検出法の王道といえる方法についてまず説明します。マイコバクテリア増殖指標試験管(MGIT, Mycobacterial Growth Indicator Tube)を用いた液体培養から始まり、固形培地への継代培養を行います。それらのサンプルに対してMALDI-TOF MSプロテオーム解析またはDNAフィンガープリンティングによって種の同定を行います。マイコバクテリアは頑丈な細胞壁を有し、薬剤標的に対する遺伝子変異や薬剤を修飾・排出する酵素を持つため、多剤耐性結核(MDR-TB)や広範耐性結核(XDR-TB)となることが多く、それにより治療が複雑にしなることもしばしばです。そのため、まずマイコバクテリアの株と既知の薬剤耐性を特定する事が重要となります。
Chinmaya Kotimoole らは、26のプロテオームデータセットから収集した7種の非結核性抗酸菌(NTM)プロテオーム解析を実施し、2000万以上のペプチドスペクトルマッチング(PSM)を取得しました。その目的は個々の種/株に特有のペプチドスペクトルライブラリを作成し、迅速な同定を可能とすることでした。様々な装置とMascot Serverを含む検索エンジンを用いて、DDAデータの解析または再解析が行われました。最終的なスペクトルライブラリとして、解析データをSkylineを経由させてBLIB形式のデータベースを得ました。
このメタ解析のデータを取得した私はその中から複数のライブラリを選定し、最近私が作成したスクリプト"blib2mspコンバーターを用いてblibからMASCOTで使用可能なMSP形式へ変換しました。20MBから4GBの範囲であった初期データベースのサイズにおいて、変換に要した時間は数分から10分程度でした。
| # | Full Species Name | MSP Library File |
|---|---|---|
| 1 | Mycobacteroides abscessus | M_abscessus_MSV000085363_20251216.msp |
| 2 | Mycobacteroides abscessus | M_abscessus_MSV000085363_FragPipe_Search_SpecLib.msp |
| 3 | Mycobacteroides abscessus | PXD022644_M_abscessus_LFQ_Proteomics_112022.msp |
| 4 | Mycobacterium avium subsp. paratuberculosis | M_avium_paratuberculosis_ProteomeDB_PD_Search_011023.msp |
| 5 | Mycobacterium kansasii | M_kansassi_Total_Proteomics_Database_Search_080122.msp |
| 6 | Mycobacteroides fortuitum | M_fortuitum_TP_FragPipe_ProteomeDB_Search_SpecLib_Final.msp |
| 7 | Mycobacterium intracellulare | M_intracellulare_TP_FragPipe_ProteomeDB_search_SpecLib.msp |
| 8 | Mycobacterium marinum | PXD003766_M_marinum_LFQ_proteomics_FragPipe_Search.msp |
| 9 | Mycolicibacterium vaccae | PASS00954_M_vaccae_Cytoplasma_CID_LFQ_Proteomics_SpecLib_112222.msp |
変換後、ライブラリ作成に使用したデータファイルとは異なるマイコバクテリアプロジェクトの質量分析データを使って検索を実行するテストを行いました。Duran Bao らの最近の研究では、異なるマイコバクテリア種および株からMRM解析用の固有ペプチドを同定し解析に利用されたことが報告されています。この研究のデータはPRIDEプロジェクト PXD059923 で公開されており、複数のNTM種由来DDAデータセットを入手する事ができました。検体は喀痰、皮膚生検、感染創傷からのぬぐい液などから採取され、BSA含有培地で培養されたサンプルです。その中で私が使用したデータは以下の通りです:
| Sample name | Expected species |
| MAB1.raw | Mycobacteroides abscessus |
| MAB10.raw | Mycobacteroides abscessus |
| MAV1.raw | Mycobacterium avium complex |
| MAV5.raw | Mycobacterium avium complex |
| MFO1.raw | Mycolicibacterium fortuitum |
| MGO1.raw | Mycobacterium gordonae |
| MINT1.raw | Mycobacterium interjectum |
| MKA1.raw | Mycobacterium kansasii |
| MMU1.raw | Mycolicibacterium mucogenicum |
| MSI1.raw | Mycobacterium simiae |
| MTB1.raw | Mycobacterium tuberculosis |
| MTB25.raw | Mycobacterium tuberculosis complex |
| MTB8.raw | Mycobacterium tuberculosis complex |
これらの検体および最初のスペクトルライブラリ生成に使用された検体には、複数のマイコバクテリウム属菌のほか、ヒトタンパク質、BSA、培養培地由来の関連ウシタンパク質も混在していました。このため種同定という目的にライブラリをそのまま追加処理なしで利用するのは好ましくありません。
そこで以前ブログ記事でご紹介した手法を再度適用し、 Unipeptを用いて対象種に特有のペプチドを選定したスペクトルライブラリ(SL)を作成する事にしました。スペクトルライブラリから全てのペプチド配列を抽出し、Unipept上で処理した後見い出された固有の代表ペプチドの情報を得て、それらのスペクトルのみを含むようライブラリを再作成しました。ライブラリからのペプチド配列抽出およびMSPライブラリのフィルタリング用スクリプトは、blib2mspコンバーター(GitHubリポジトリ)に含まれています。これは内容的にはChinmaya Kotimoole et al.がライブラリ作成時に使用したプロセスと同じですが、彼らは独自のツールを作成し利用しておりその点で異なります。私が適用したフィルタリングルールは単純です:
# Extract from MSP file perl extract_peptides.pl -i my_library.msp # Output: my_library_peptides.txt # Filter MSP file (auto-generates output filename) perl filter_msp.pl -i library.msp -p peptide_list.txt # Output: library_filtered.msp
Bao et al.のデータファイルの一部をMascot Distillerで処理し、異なるMycobacteriaスペクトルライブラリ(SL)、UnipeptでフィルタリングしたSL、 UnipeptでフィルタリングしたSLにPRIDE_ContaminantsデータベースおよびPRIDE_Humanデータベースを追加したもの、SLとUniprot Mycobacteriaceae FASTAファイル(organism_id:1762)を組み合わせたもの、そしてUniprot Mycobacteriaceae FASTAファイルのみ、というデータベースまたはライブラリを検索対象として準備しました。ライブラリを使用する場合、修飾は元の解析およびライブラリ生成時に既に含まれているため検索パラメーターとして修飾設定を追加する必要はありません。FASTAファイルを含む検索では、固定修飾としてシステインのカルバミドメチル化、可変修飾としてタンパク質N末端のアセチル化、メチオニンの酸化を使用しました。またペプチド質量の許容誤差は±20 ppm、フラグメント質量の許容誤差は±0.6 Daと設定しました。検索を実施した際の検索時間(16コアが使用可能なライセンス)で、サンプルファイルのサイズにより異なりましたが、全スペクトルの複数ライブラリ検索で1~5分、Uniprot Mycobacteriaceae FASTAファイルを含む検索では3~11分でした。
解析結果
統合スペクトルライブラリに対する検索は同定基準を超えるペプチドをレポートしたものの、マッチングが期待された種との比較という点ではあまり満足のいく結果にはなりませんでした。
データベース検索では統計的有意性を検証可能なp値とともに、データベース内のペプチドに対して最も良いスコアでマッチした内容が報告されます。フィルタリング前のスペクトルライブラリに対する検索では多くのマッチングが得られたものの、種特有のペプチドに対するマッチはごくわずかでした。フィルタリング済みのライブラリに対する検索においてマッチング数が減少し、マッチしてもその多くが最大のスペクトルライブラリでマッチするという結果の偏りが見られました。今回の解析対象ではない種のサンプルデータは解析対象種が検出されないことが望ましいネガティブコントロールとしてみることができます。元の論文のように種同定の確度を高めるには、利用可能な全ライブラリを変換・フィルタリング・検索し、ライブラリ内の全種を代表し十分な固有ペプチドを確保する必要があります。
ライブラリに対する結果に比べると、FASTAファイルへの通常のデータベース検索はよい結果を示しました。Mascotの検索結果レポートから同定されたペプチドを出力し、Unipeptで最下位共通祖先(LCA, Lowest Common Ancestor)レポートを生成しました。
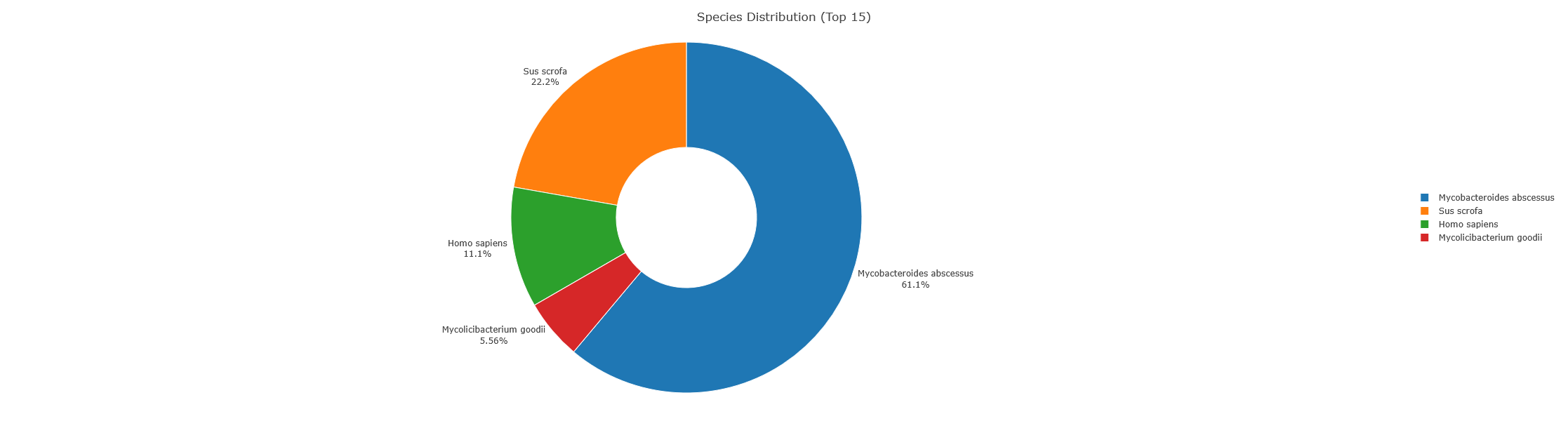
サンプルMAB10.rawはMycobacteroides abscessusと容易に同定できました。LCAとみなされた全218ペプチドのうち、18(8.3%)が4種の固有種レベルまで同定されました。残りの200個(91.7%)のペプチドは複数の生物種においてマッチしたため、より上位の分類レベル(属、科、目など)として割り当てました。
Top 5 の種 - MAB10
- Mycobacteroides abscessus (species): 11 peptides (5.0%)
- Sus scrofa (species): 4 peptides (1.8%)
- Homo sapiens (species): 2 peptides (0.9%)
- Mycolicibacterium goodii (species): 1 peptides (0.5%)
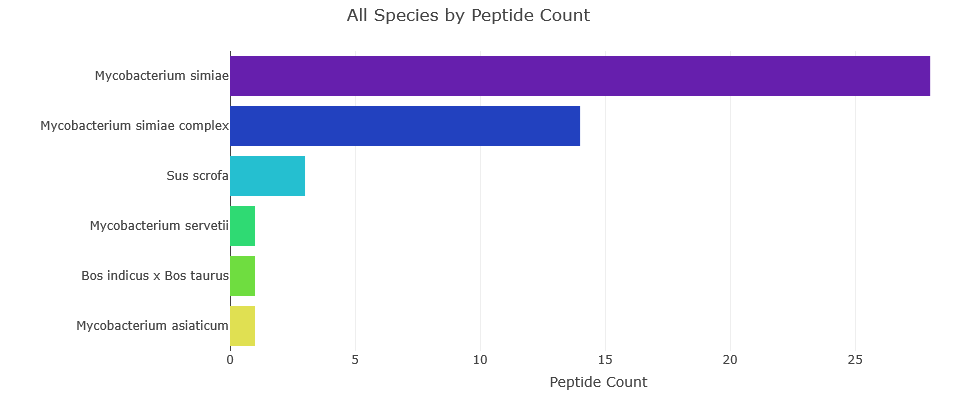
サンプル MSI1.raw については、検索対象となる Mycobacterium simiae のライブラリデータが存在せず、最大のライブラリである Mycobacterium fortuitum と 1 件のみマッチングが確認されました(そのためおそらく偽陽性と考えられます)。一方FASTA ファイルに対する通常の検索では330 個のペプチドが同定され、最も多くの固有ペプチド(合計 42 個)を有する種はMycobacterium simiae およびその複合種群でした。
Top 5 の種 - MSI1
- Mycobacterium simiae (species): 28 peptides (8.5%)
- Mycobacterium simiae complex (species group): 14 peptides (4.2%)
- Sus scrofa (species): 3 peptides (0.9%)
- Mycobacterium servetii (species): 1 peptides (0.3%)
- Bos indicus x Bos taurus (species): 1 peptides (0.3%)
Mycobacterium avium 複合体はサンプルMAV1.rawおよびMAB10.rawで同定されましたが、MAV5.rawからは非結核性抗酸菌(NTM)種が同定されませんでした。MGO1.rawサンプルに対しても、Mycobacterium属特有のペプチドマッチングが確認されませんでした。Mycobacterium tuberculosis の全サンプルは正しく同定され、Mycolicibacterium mucogenicumも同様に同定されました。最後に、MKA1.rawサンプルではMycobacterium kansasiiに対する固有ペプチドマッチングが認められませんでしたが、 Mycolicibacterium fluoranthenivorans に対する固有ペプチドマッチングは確認できました。
上記はサンプル中の種存在を統計的有意性による判断基準を適用しています。ただし、有意基準までには達していないというのは対象種がサンプルに存在しないことを証明するわけではなく、単に有意基準を超えるまでの証拠を持つものが検出されなかった事を意味します。今回の解析はPEP-TORCHアルゴリズムと同等というわけではなく、より簡便な代替手法となるかもしれません。
今回のスペクトルライブラリ検索の結果は芳しくなく、さらに多くのライブラリの変換とフィルタリングからより大規模なライブラリを作成する必要がある事が示唆されました。一方通常のデータベースと一緒に行ったライブラリ検索は、ある程度期待通りに機能したのではないでしょうか。
Keywords: metaproteomics, spectral library